

01研究介紹
真核細胞通過一種分級的DNA-蛋白質(zhì)組裝壓縮方式届氢,將長達2米的基因組DNA包裝在一個直徑為幾微米的細胞核中闺金。第一級是核小體徊极,由147 bp的DNA包裹在四個核心組蛋白(H2A掐股、H2B院颜、H3和H4)構(gòu)成的八聚體上組成拇舀。然后瞎暑,核小體的這個基本重復(fù)單元被組織成 10 納米的“串珠”染色質(zhì)纖維曙求,進一步壓縮成更高階的染色質(zhì)結(jié)構(gòu),以適應(yīng)微米大小的細胞核度气。染色質(zhì)的組織受到大量化學(xué)修飾的調(diào)控割按,特別是在組蛋白核心蛋白的N端尾部,如乙趿准化和甲基化适荣。組蛋白修飾調(diào)節(jié)核小體包裝成高階染色質(zhì)結(jié)構(gòu),以影響基因組DNA對轉(zhuǎn)錄機制蛋白的可及性院领。隨后弛矛,不同表觀基因組狀態(tài)下的染色質(zhì)壓縮控制著它們的基因表達,并對許多細胞過程產(chǎn)生顯著影響比然,如DNA復(fù)制丈氓、細胞分裂、DNA損傷和DNA修復(fù)强法。
不同的組蛋白修飾如何在每個表觀基因組狀態(tài)下塑造高階染色質(zhì)結(jié)構(gòu)仍然是一個重要的問題万俗。由于傳統(tǒng)光學(xué)顯微鏡的分辨率有限,目前對不同組蛋白修飾定義的高階染色質(zhì)結(jié)構(gòu)的理解是通過體外生化分析間接推斷出來的梭唆,如染色質(zhì)免疫沉淀(ChIP)辆泄。這些分析通常依賴于對來自聚集細胞群的片段DNA的分析,并在單細胞水平上丟失信息踱陡。目前铐坠,超分辨率熒光顯微鏡的最新進展使在固定細胞和活細胞中進行低于衍射有限分辨率的染色質(zhì)結(jié)構(gòu)成像成為可能≥┰荆基于定位的超分辨率顯微鏡遂涛,如(直接)隨機光學(xué)重建顯微鏡(STORM)提供了一種最佳的空間分辨率,直接可視化以前不可見的高階染色質(zhì)結(jié)構(gòu)甚至光學(xué)分辨率20-30納米的體內(nèi)單細胞核柄露。超分辨率成像顯示醉檐,體內(nèi)染色質(zhì)結(jié)構(gòu)由異質(zhì)的核小體簇組成,以及特定基因位點不同表觀基因組狀態(tài)的不同染色質(zhì)包裝奥怪。然而勿镇,由不同的組蛋白修飾形成的原位全基因組的高階染色質(zhì)結(jié)構(gòu)仍然難以捉摸。
研究關(guān)注由組蛋白乙跖糖疲化和甲基化標(biāo)記定義的全基因組高階染色質(zhì)結(jié)構(gòu)的全面原位特征蚂兴,以及它們的空間鄰近性柒浙,通過STORM共同形成單個哺乳動物細胞核的染色質(zhì)環(huán)境。我們選擇了一組10個組蛋白標(biāo)記章姓,包括參與活性轉(zhuǎn)錄的賴氨酸乙跫亚玻化和參與抑制和活躍轉(zhuǎn)錄的賴氨酸甲基化。研究的超分辨率成像和定量分析揭示了高階染色質(zhì)的三個主要結(jié)構(gòu)特征:組蛋白乙醴惨粒化形成空間分離的核小體納米團簇零渐,活性組蛋白甲基化形成空間分散的核小體納米域,抑制性組蛋白甲基化形成高度濃縮的大聚集體系忙。雙色STORM成像顯示诵盼,轉(zhuǎn)錄活性組蛋白標(biāo)記與“開放”染色質(zhì)一致,轉(zhuǎn)錄抑制組蛋白標(biāo)記與高度濃縮的染色質(zhì)一致银还。進一步對它們的空間鄰近性的研究表明风宁,抑制性和活性組蛋白標(biāo)記大多具有空間排他性,而在活性組蛋白標(biāo)記中可以觀察到相當(dāng)多的共定位蛹疯。綜上所述戒财,超分辨率成像有助于揭示組蛋白乙酰化和甲基化是如何在單個哺乳動物細胞核的水平上捺弦,在從幾十納米到幾微米的尺度上形成高階染色質(zhì)結(jié)構(gòu)的饮寞。
02研究結(jié)果(節(jié)選)
1、不同組蛋白標(biāo)記的STORM圖像和定量表征
作者可視化了由哺乳動物細胞核中10個組蛋白修飾所定義的全基因組高階染色質(zhì)結(jié)構(gòu)脂槽。圖1A-1C顯示了來自10個組蛋白標(biāo)記的代表性寬場和超分辨率圖像拜岂,包括轉(zhuǎn)錄活性組蛋白乙酰化標(biāo)記(H3K9ac妨宙、H3K27ac矫摸、H3ac和H4ac)耗砖、轉(zhuǎn)錄活性組蛋白甲基化標(biāo)記(H3K4me1伐歇、H3K4me2、H3K4me3和H3K36me3)和轉(zhuǎn)錄抑制組蛋白甲基化標(biāo)記(H3K27me3和H3K9me3)廉旅。圖1A和1B的超分辨率圖像顯示了明顯的結(jié)構(gòu)特征:組蛋白乙醮乓觯化標(biāo)記形成空間分離和離散的核小體納米團簇,和組蛋白甲基化標(biāo)記形成高度異質(zhì)和空間分散的核小體納米域桌苔。圖1C的寬視場圖像中顯示了抑制標(biāo)記(H3K27me3和H3K9me3)在細胞核內(nèi)呈濃縮的聚集物革睬。超分辨率的圖像清楚地顯示了在核、核仁和核漿外圍的高度濃縮(幾百納米)中腻喇,有甚至是超大(微米大锌⒖怠)團核的存在。圖1D顯示了圖1A-1C中選定的超分辨率圖像區(qū)域中三個代表性組蛋白標(biāo)記(H3K9ac瓢谢、H3K4me1和H3K27me3)的總體分布圖畸写,它清楚地顯示了高階染色質(zhì)結(jié)構(gòu)的三個明顯特征驮瞧。
作者量化了每個組蛋白標(biāo)記所形成的這些結(jié)構(gòu)特征。圖1E顯示枯芬,組蛋白乙趼郾剩化標(biāo)記在小于50 nm的短長度尺度上表現(xiàn)出狹窄的尖峰,表明存在高度聚集的小納米結(jié)構(gòu)千所;組蛋白甲基化標(biāo)記的RDF分布更廣狂魔,表明存在更大的聚物和更長的相關(guān)長度。進一步量化由不同組蛋白標(biāo)記形成的納米團簇和納米結(jié)構(gòu)域的大小淫痰,圖1F顯示了平均大小與SD的散點圖最楷。
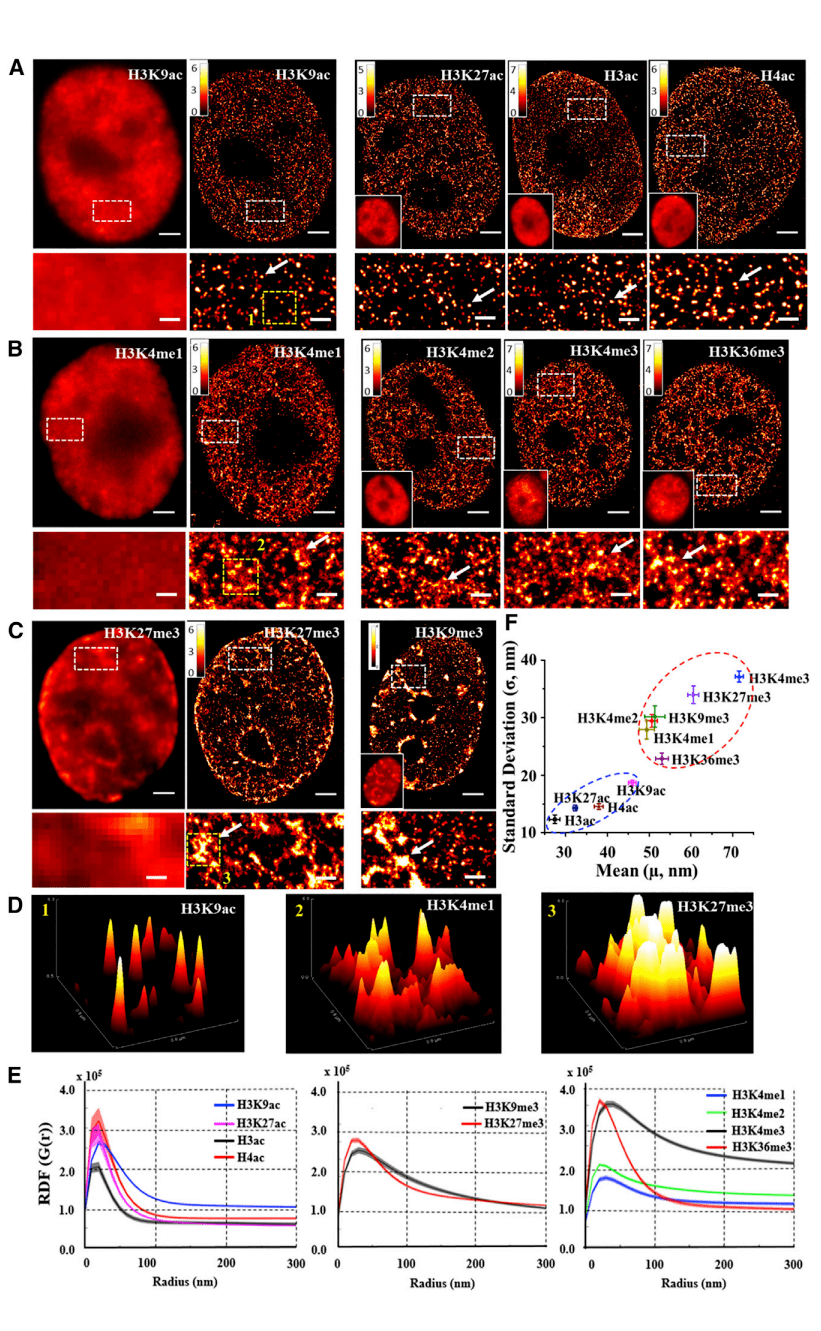
圖1
2、間期細胞核中不同組蛋白標(biāo)記和 DNA 的雙色STORM圖像
作者通過雙色STORM成像觀測到組蛋白標(biāo)記和DNA之間的空間關(guān)系黑界。圖 2 顯示了轉(zhuǎn)錄活性或抑制性組蛋白標(biāo)記(綠色管嬉,用 Cy3B 標(biāo)記)和 DNA(紅色,用 Alexa Fluor 647 標(biāo)記)的代表性超分辨率圖像朗鸠,以及它們的合并圖像和共定位點(用白色標(biāo)記 )蚯撩。這些圖像顯示,DNA在細胞核中高度緊湊形成了分隔區(qū)域抵刺,其中饲悟,H3K9ac或H3K4me3的活性組蛋白標(biāo)記在DNA較不致密的區(qū)域更為豐富(圖2A和2B),而H3K27me3的抑制性組蛋白標(biāo)記大多與DNA的濃縮區(qū)域相一致(圖2C)衫喜。這一直接的視覺證據(jù)顯示了組蛋白標(biāo)記和染色質(zhì)致密度之間的關(guān)系:抑制性組蛋白標(biāo)記與高度濃縮的染色質(zhì)結(jié)構(gòu)有關(guān)根朱,而活性組蛋白標(biāo)記與更多的“開放”或更少致密的染色質(zhì)結(jié)構(gòu)有關(guān)。
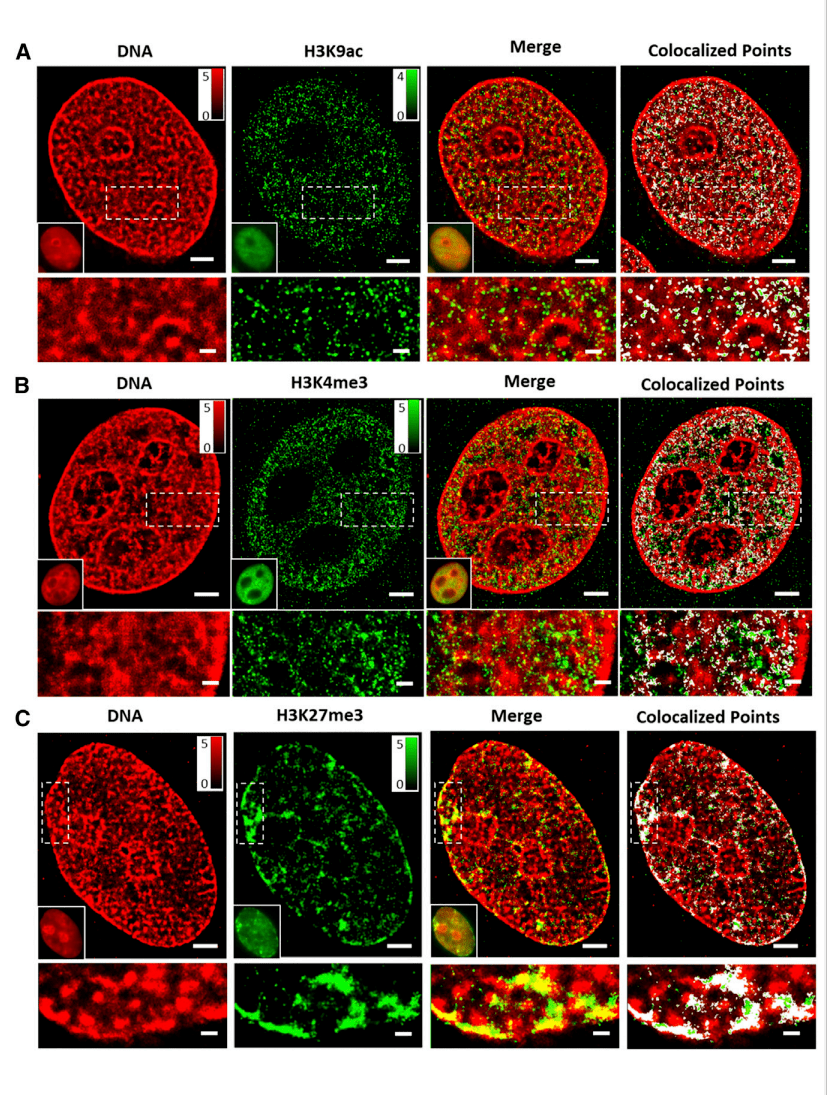
圖2
03研究總結(jié)
作者展示了超分辨率定位顯微鏡STORM在間期哺乳動物細胞核中的表觀基因組狀態(tài)下直接可視化全基因組高階染色質(zhì)結(jié)構(gòu)的潛力可丝。研究結(jié)果揭示了由組蛋白乙趺艉校化和甲基化標(biāo)記形成的高階染色質(zhì)結(jié)構(gòu)的先前看不見的獨特特征。這一結(jié)果為未來研究這些結(jié)構(gòu)特征的功能意義以及它們在不同疾病狀態(tài)下如何改變奠定了基礎(chǔ)氓愿。
04超高分辨率顯微成像系統(tǒng)iSTORM
前文中提及的STORM成像技術(shù)翁凳,目前已成功實現(xiàn)商用,有需要STORM成像技術(shù)進行實驗研究的專家老師們咪轩,請溝通對接預(yù)約哦
超高分辨率顯微成像系統(tǒng) iSTORM县趴,成功實現(xiàn)了光學(xué)顯微鏡對衍射極限的突破,使得在 20 nm的分辨率尺度上從事生物大分子的單分子定位與計數(shù)涉粘、亞細胞及超分子結(jié)構(gòu)解析锭汛、生物大分子生物動力學(xué)等的研究成為現(xiàn)實,從而給生命科學(xué)袭蝗、醫(yī)學(xué)等領(lǐng)域帶來重大性突破 唤殴。

圖2、超高分辨率顯微成像系統(tǒng)iSTORM。
超高分辨率顯微成像系統(tǒng) iSTORM 具有 20 nm超高分辨率朵逝、3通道同時成像腺兴、3D同步拍攝、實時重構(gòu)廉侧、2小時新手掌握等特點页响,已實現(xiàn)活細胞單分子定位與計數(shù),并提供熒光染料選擇段誊、樣本制備闰蚕、成像服務(wù)與實驗方案整體解決方案, 以納米級觀測精度连舍、高穩(wěn)定性没陡、廣泛環(huán)境適用、快速成像审亿、簡易操作等優(yōu)異特性焊循,獲得了超過50家科研小組和100多位科研人員的高度認可。
參考文獻:
Xu J , Ma H , Jin J , et al. Super-Resolution Imaging of Higher-Order Chromatin Structures at Different Epigenomic States in Single Mammalian Cells[J]. Cell Reports, 2018, 24(4):873.



